اسید نیتریک که به نام های تیزاب یا جوهر شوره نیز شناخته می شود یک اسید معدنی بسیار قوی با فرمول شیمیایی HNO3است . اسید نیتریک خالص بی رنگ است اما نمونه های قدیمی تر به دلیل تجزیه به اکسیدهای ازت و آب،زرد رنگ هستند
اسید نیتریک در آب محلول است و همچنین یک ماده اکسید کننده قوی است که بسیار خورنده و سمی باشد. این ماده با فلزات ، اکسیدها و هیدروکسیدها واکنش نشان می دهد و نمک های نیترات را تشکیل می دهد.
این اسید دود کننده و بسیار خورنده با نقطه انجماد ۴۲- درجه سانتی گراد ونقطه جوش ۸۳ درجه سانتیگراد است و یک معرف آزمایشگاهی رایج و مهم صنعتی است. این ماده در دمای معمولی نیز کمی تجزیه می شود و گرم شدن یا قرارگرفتن در معرض نور مستقیم خورشید باعث تجزیه بیشتر آن می شود و در نتیجه رنگ آن به زرد یا قهوه ای تغییر می یابد.
اسید نیتریک با اکثر فلزات ، به جز طلا و پلاتین ، برای تولید نیترات واکنش نشان می دهد.استفاده اصلی از اسید نیتریک (۸۰٪) در تولید کودهای کشاورزی است. از کل تولیدات این ماده ۹۶٪ برای تهیه نیترات آمونیوم و نیترات کلسیم آمونیوم استفاده می شود. برای ساخت مواد منفجره از مقدار نسبتاً کمی نیترات آمونیوم استفاده می شود.
اسید نیتریک معمولاً با اکسیداسیون آمونیاک به دست می آید. این کار عمدتا با استفاده از فرآیند Ostwald انجام می شود. این اسید همچنین با تیمار نیترات سدیم با اسید سولفوریک نیز تولید می شود ولی این روش بازدهی کمی دارد
این ماده در ساخت نیترات معدنی و آلی و ترکیبات نیتروژن برای کودها ، واسطه های رنگ ، مواد منفجره و بسیاری از مواد شیمیایی آلی مختلف استفاده می شود.اسید نیتریک ماده ای بسیار مهم است که به عنوان ماده اولیه برای تولید مواد دیگر استفاده می شود.
این امر باعث اهمیت آن در صنایع شیمیایی و دارویی می شود. این اسید همچنین جزئی از باران های اسیدی است و به عنوان یک ماده
اکسید کننده قوی در موشک ها به عنوان سوخت مایع مورد استفاده قرار گرفته است.محلول ۷۰% معمولا به عنوان اسید نیتریک غلیظ از نظر تجاری در دسترس است غلظت های بالاتر از ۹۰٪ را اسید نیتریک دود کننده می گویند
در تماس با هوااسید نیتریک دود کننده ، دودهای سفید یا قرمز بسیار سمی ، خورنده و واکنش پذیر با مواد قابل احتراق تولید می کند.
اسید نیتریک در لفظ انگلیسی :( nitric acid ) یک ماده شیمیایی معدنی به صورت مایعی با بوی ملایم و تند است. غلظت های مختلفی از این ماده وجود دارد که می توان از آنها استفاده کرد. بنابراین، بی رنگ،زرد یا قرمز است. گرید صنعتی حدود ۶۸ درصد در آب، گرید تجاری بین ۵۲ تا ۶۸ درصد و اسید نیتریک دوددار ۸۶ درصد است.
غلظت بالای ۹۵٪، اسید نیتریک دوددار زرد سفید بخار نامیده می شود. این ماده یک اسید مونوپروتیک قوی است
این ماده , آمونیاک، ماده اولیه اصلی را تحت یک کاتالیزور پلاتین اکسید می کند. این اسید یک اسید معدنی پایه است که به طور گسترده در صنعت استفاده می شود
به راحتی هیدرات های جامد مانند HNO3 H2O و HNO3 3H2O را تشکیل می دهد. می تواند توسط گرما یا نور تجزیه شود

نام های دیگر اسید نیتریک
اسید نیتریک را با نام های دیگری نظیر ازوتیک اسید، نیترات هیدروژن یا هیدروژن نیترات، اسید ازوتیک، جوهر شور، اسید ازته، نیتروکسید آنیل نیز می شناسند.
اسید نیتریک و زنجیره ارزش آن
کاربردهای اسید نیتریک
کاربرد اسید نیتریک در خالص سازی فلزات
در بازیافت پلاتین از اسید نیتریک استفاده می شود و باتوجه به این که تمامی نیترات های فلزات محلول هستند
از این طریق می توان، اورانیوم خالص را تهیه کرد که در نیروگاه های اتمی مصرف می شود. در استخراج طلا و در بازیافت ضایعات الکترونیک نیز از اسید نیتریک استفاده می شود.
کاربرد اسید نیتریک در کشاورزی
بیشترین مصرف نیتریک اسید در تهیه کودهای شیمیایی ( کشاورزی) از قبیل کودهای نیترات ( نیترات کلسیم، نیترات آمونیوم و غیره) است. ساخت کودهای شیمیایی نیتروژن دار مانند: اوره، آمونیوم نیترات، نیتروفسفات، کودهای مخلوط و غیره می باشد.
کاربرد اسید نیتریک در موادمنفجره و مهمات
به دلیل قدرت اکسیدکنندگی زیاد نیتریک اسید، در حین تماس با ترکیباتی مانند سیانیدها و کاربیدها سبب انفجار می شود. از دیگر مصارف این اسید تولیدموادی مانند: سایکلو تری متیلن تری نیترامین، ماده منفجره مانند نیتروگلیسیرین و تری نیتروتولوئن می باشد.
در تولید نیترات های معدنی (نیترات آمونیوم انفجاری) و آلی از نیتریک اسید به وفور استفاده می شود.
کاربرد اسید نیتریک در سوخت مایع شاتل ها
از دیگر مصارف اسید نیتریک ۱۰۰ درصد استفاده از آن به عنوان اکسیدکننده درسوخت مایع شاتل های فضایی موشک، سوخت مایع در رشته مهندسی هوافضا و همچنین در راکت ها است و از اسید نیتریک بالای ۸۵ درصد (اسید نیتریک قرمز) به همراه اسید سولفوریک به عنوان اکسیدکننده استفاده می شود.
کاربرد اسید نیتریک در تهیه تیزاب
در تهیه” تیزاب سلطانی” و یا نیترو هیدروکلریک اسید (ترکیب اسید نیتریک غلیظ با هیدروکلریدریک اسید غلیظ) از اسید نیتریک استفاده می شود. این ماده خاصیت دودکننده و خورنده زرد یا قرمز دارد.
کاربرد اسید نیتریک در تصفیه نانو لوله ها
برای تولید گروه های عاملی روی سطح نانولوله های کربنی، آن ها در محیط آبی به صورت کاملا هموژن دیسپرس می کنند. به همین خاطر ابتدا نانولوله های کربنی در محیط های اسیدی مختلف ازقبیل اسید نیتریک، اسید سولفوریک و اسیدکلریدریک دیسپرس می کنند.
کاربرد اسید نیتریک در تمیزکاری و اسیدشویی
همچنین (۵ تا ۳۰) درصد اسید نیترتیک به همراه (۳۰ تا ۴۰) درصد اسید فسفریک برای تمیز کردن رسوبات، ترکیبات کلسیمی و منیزیمی روی ظروف خوراکی و لبنیات استفاده می شود. از دیگر ویژگی های اسید نیتریک خورندگی بالا و حلالیت بالا (فلزات به راحتی در خود حل می کند) می باشد و این اسید در شست و شو نیز کاربرد فراوانی دارد.
کاربرد اسید نیتریک در صنایع غذایی
برای جلوگیری از رشد باکتری ها و مسمومیت های غذایی کشنده در این فراورده ها از یون نیتریت استفاده می شود. این ماده به عنوان افزودنی به گوشت تازه و برای ثابت ماندن رنگ گوشت قرمزمصرف می شود. به همین دلیل گوشت های قرمز تازه ای که خریداری می کنید لزوما کشتار روز نیستند و ممکن است مقداری نیتریت به آن افزوده باشند.
به عنوان نگهدارنده در فرآیند پردازش گوشت هایی مانند: سوسیس، کالباس، انواع بیف ها، بیکن ها، همبرگر و… مورد استفاده قرار می گیرند.
روش تولید
امروزه روش های مختلفی برای تولید اسید نیتریک وجود دارد که از آن جمله می توان به روش بریک لند و روش استوالد اشاره کرد که از بهترین و قدیمی ترین روش ها هستند. روش های تولید صنعتی اسید نیتریک به طور خلاصه به شرح زیر است:
روش اول
واکنش نیترات پتاسیم یا سدیم با اسید سولفوریک که باعث تقطیر نیترات پتاسیم و تولید اسید نیتریک می شود. این واکنش فوق العاده گرمازا است و دمایی در حدود 900 درجه سانتیگراد ایجاد می کند و اسید به صورت بخار خارج می شود. این روش تولید اسید نیتریک دارای معایبی است. اولاً به منبع سوخت بالایی نیاز دارد، در حالی که باعث فرسودگی تجهیزات می شود و اسید به اکسیژن، آب و اکسید تبدیل می شود. البته برای حل این مشکلات دو واکنش دهنده به نسبت مساوی با هم ترکیب می شوند.
روش دوم
در روش دوم که روش بریک لند نام دارد در کوره های خالص اکسیژن و نیتروژن با هم واکنش می دهند و گاز دی اکسید نیتروژن تولید می شود و سپس جذب آب می شود و اسید نیتریک تولید می کند. این روش به ندرت مورد استفاده قرار می گیرد زیرا توجیه اقتصادی ندارد.
روش سوم
روشی که امروزه برای تولید اسید نیتریک استفاده می شود، سنتز آن از آمونیاک است. در این واکنش آمونیاک با اکسیژن ترکیب شده و اسید نیتریک بدست می آید. در این روش، آمونیاک با اکسیژن هوا به اکسید نیتروژن تبدیل می شود. مراحل تولید را در تصویر زیر مشاهده می کنید. سپس با استفاده از یک کاتالیزور آلیاژ پلاتین-رودیوم، NH3 به NO اکسید می شود. پس از این مرحله معمولاً با استفاده از نیترات منیزیم اسید نیتریک تولید می شود.
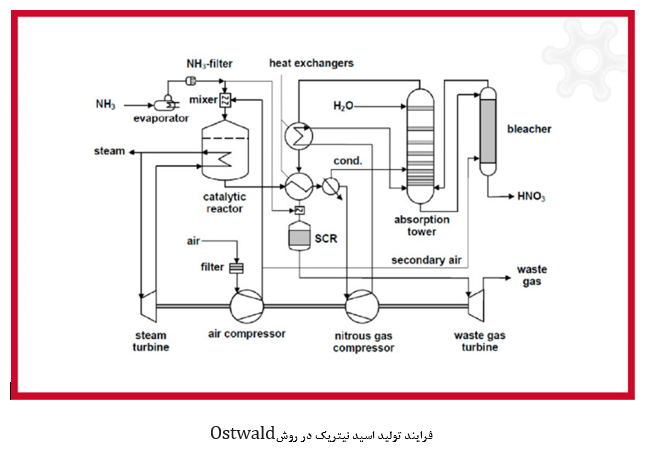
تهیه شده در گروه مطالعات راهبردی سپینود شرق
زمستان1402









